4 juin 2020
4
04
/06
/juin
/2020
09:53
benzopinacol
ou
1,1,2,2-tétraphényléthane-1,2-diol
Méthodes Ciamician et Gilbert - 1900 et Cohen - 1920
réaction de réduction photochimique

Mode opératoire:
1/ Dans un erlenmeyer de 100 cm3 dissoudre 2.0 g de benzophénone dans 15 cm3 de propan-2-ol, tout en agitant et chauffant doucement au bain-marie. Ajouter 1 cm3 d'acide éthanoïque pur.
2/ Transvaser dans un tube en quartz et l'exposer aux rayonnements d'une lampe à ultraviolet pendant 180 minutes. Le benzopinacol, insoluble dans le propan-2-ol, se forme sur les parois de quartz.
3/ Agiter le contenu du tube de quartz et filtrer sur fritté. Sécher pendant 15 minutes par aspiration.
benzophénone: 
Published by jeanlouis.migot
-
dans
synthèse
1 juin 2020
1
01
/06
/juin
/2020
09:17
2-acétylcyclohexanone

Mode opératoire:
1/ Dans un ballon tricol de 500 cm3 équipé d'une ampoule de coulée, verser 25 cm3 de N-morpholino-1-cyclohexène (Voir Synthèse - 180), 15 cm3 de triéthylamine et 120 cm3 de dichlorométhane. Agiter et chauffer le mélange jusqu'à 35°C. Verser 7.0 g de chlorure d'éthanoyle dans l'ampoule de coulée et introduire au goutte à goutte, la température ne doit pas dépasser 40°C. Agiter pendant 240 minutes en maintenant la température entre 35 et 40°C. Verser 25 cm3 d'acide chlorhydrique puis 20 cm3 d'eau tout en agitant. Chauffer à reflux pendant 120 minutes.
2/ Laisser refroidir le milieu réactionnel puis verser dans une ampoule à décanter de 1000 cm3. Recueillir la phase organique et laver à l'eau jusqu'à ce que le pH soit proche de 5. Sécher sur du sulfate de magnésium anhydre. Concentrer à l'évaporateur rotatif. Distiller sous pression réduite.
N-morpholino-1-cyclohexène:

Published by jeanlouis.migot
-
dans
synthèse
29 mai 2020
5
29
/05
/mai
/2020
11:05
tétraphénylcyclopentadiénone
ou
2,3,4,5-tétraphényl-2,4-cyclopentadien-1-one
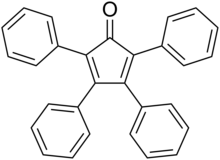
méthode Dilthey - 1930
Mode opératoire:
1/ Sous une hotte aspirante, dans un monocol de 100 cm3, introduire 4.0 g de benzile, 4.0 g de dibenzylcétone puis 30 cm3 d'éthanol chaud. Installer un réfrigérant à boules et agiter jusqu'à dissolution.
2/ Chauffer au bain-marie quasi à ébullition. Ajouter par l'extrémité supérieure du réfrigérant à boules une solution de 0.7 g d'hydroxyde de potassium dans 7 cm3 d'éthanol. Chauffer à reflux pendant 20 minutes. Refroidir le contenu du ballon dans un bain de glace. Filtrer sur fritté et laver avec 20 cm3 d'éthanol. Sécher par aspiration.
3/ Recristalliser dans un mélange toluène-éthanol 1-1.
benzil: 
dibenzylcétone: 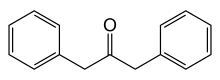
Published by jeanlouis.migot
-
dans
synthèse
28 mai 2020
4
28
/05
/mai
/2020
13:08
dicinnamalacétone
ou
1,9-diphényl-1,3,6,8-nonatétraèn-5-one
méthode Diehl - Einhorn - 1885
réactions d'aldolisation et de crotonisation

Mode opératoire:
1/ Verser dans un erlenmeyer de 100 cm3 25cm3 d'éthanol puis 4 cm3 de cinnamaldéhyde. Agiter pour homogénéiser la solution. puis verser 15 cm3 d'hydroxyde de sodium 2M.
2/ Tout en maintenant l'agitation, additionner en une seule fois 1 cm3 de propanone. Agiter pendant 20 minutes. Filtrer sur verre frité. Laver avec 20 cm3 d'éthanol et sécher par aspiration avec la trompe à eau.
cinnamaldéhyde: 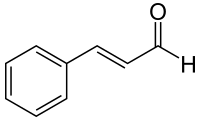
Published by jeanlouis.migot
-
dans
synthèse
28 mai 2020
4
28
/05
/mai
/2020
10:20
4-méthylpent-3-ène-2-one
ou
oxyde de mésityle
(voir Synthèse - 23)
méthode Hoffman - 1909

Mode opératoire:
1/ dans un ballon monocol de 250 cm3, introduire 120 cm3 de propanone et quelques grains de pierre ponce. Réaliser un montage Soxhlet et remplir la cartouche avec de la baryte hydratée (BaO). Alimenter le réfrigérant à boules. Chauffer de manière à distiller au moins 5 fois la propanone. Refroidir ensuite le ballon monocol.
2/ Distiller le produit brut obtenu (bp = 130°C).
Published by jeanlouis.migot
-
dans
synthèse
27 mai 2020
3
27
/05
/mai
/2020
15:01
Emil Knoevenagel
1865 - 1921

Published by jeanlouis.migot
-
dans
théorie
27 mai 2020
3
27
/05
/mai
/2020
14:31
1-phényl-4,4-dicyanobutadiène
C6H5-CH=CH=CH=C(CN)2
réaction de Knoevenagel - 1894 (voir Théorie -38)
Mode opératoire:
1/ Dans un erlenmeyer de 50 cm3 contenant 10 cm3 d'éthanol, introduire 1.25 cm3 de cinnamaldéhyde et agiter avec un agitateur magnétique afin d'homogénéiser la solution. Introduire 0.65 g de malonodinitrile et agiter à température ambiante jusqu'à disparition du réactif.
2/ Ajouter 1 goutte de pipéridine et agiter pendant 15 minutes. Un précipité jaune apparait. Filtrer sur verre fritté. Laver le précipité avec 10 cm3 d'éthanol et sécher pas aspiration avec la trompe à eau. Le filtrat précédent peut donner lieu à une deuxième cristallisation qui doit subir le même traitement que précédemment.
cinnamaldéhyde: 
malonodinitrile: 
pipéridine: 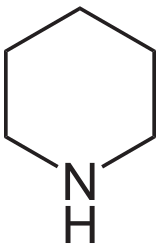
:
Published by jeanlouis.migot
27 mai 2020
3
27
/05
/mai
/2020
13:56
résine urée-formol
ou
résine urée-méthanal

Mode opératoire:
1/ Préparer une solution de 10.0 g d'urée et de 15 cm3 d'acide chlorhydrique concentré dans 100 cm3 d'eau.
2/ Verser 10 cm3 d'une solution de méthanal à 35%. Agiter avec une baguette de verre. La résine, gorgée d'eau, se présente sous la forme d'un gel, structure tridimensionnelle.Il est conseillé de la transférer, avec précaution, dans un récipient jetable avant qu'elle ne prenne en masse.
urée: 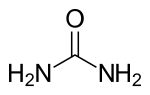
méthanal: 
Published by jeanlouis.migot
-
dans
synthèse
25 mai 2020
1
25
/05
/mai
/2020
16:35
benzaldéhyde

Mode opératoire:
1/ obtention du bromure de phénylmagnésium C6H5MgBr: addition lente, dans un tricol de 500 cm3, et sous agitation d'une solution de 20.0 g de bromobenzène (C6H5Br) sur 3.0 g de magnésium recouvert de 60 cm3 de diéthyléther. Puis amorçage de la réaction par un chauffage doux. Refroidir le tricol dans un bain de glace.
2/ Ajouter 16.0 de triéthoxyméthane (ou orthoformiate d'éthyle) en 15 minutes. Chauffer à reflux pendant 90 minutes. Refroidir puis installer à la place du réfrigérant à boules un montage à distiller. Distiller l'éther.
triéthoxyméthane: 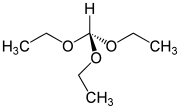
3/ Verser dans le tricol une solution contenant 10 cm3 d'acide chlorhydrique concentré et 30 cm3 d'eau. Rajouter 30 cm3 si la solution n'est pas limpide. Extraire la phase aqueuse avec 3 portions de 40 cm3 d'éther. Rajouter 20 cm3 dans la phase organique puis avec 20 cm3 d'une solution d'hydrogénocarbonate de sodium à 5%. Sécher la phase organique avec 8.0 g de sulfate de magnésium anhydre. Distiller le solvant à l'évaporateur rotatif. Distiller le produit pur sous pression réduite éventuellement.
Published by jeanlouis.migot
-
dans
synthèse
18 mai 2020
1
18
/05
/mai
/2020
16:54
4-nitrosodiméthylaniline

Mode opératoire:
1/ Dans un erlenmeyer de 100 cm3 verser 30 cm3 d'eau puis, avec précaution, 20 cm3 d'acide chlorhydrique concentré. Verser 8.0 g de N,N-diméthylaniline. Refroidir dans un bain de glace (Solution 1).
2/ Dissoudre 4.7 g de nitrite de sodium dans 5 cm3 d'eau. Puis verser cette solution, lentement, à la Solution 1. Continuer l'agitation pendant 15 minutes.
3/ Filtrer sur Büchner et laver avec 40 cm3 d'acide chlorhydrique dilué. Mettre le solide en suspension dans 50 cm3 d'eau et verser de l'hydroxyde de sodium dilué jusqu'à neutralisation. Verser dans une ampoule à décanter. Extraire la phase aqueuse en deux fois avec 20 cm3 d'éther. Rassembler les phases organiques. Sécher sur du sulfate de sodium anhydre. Filtrer et évaporer du filtrat le solvant à l'évaporateur rotatif. Laisser cristalliser. Filtrer sur fritté pour récupérer le produit final.
Published by jeanlouis.migot
-
dans
synthèse


























