23 mars 2021
2
23
/03
/mars
/2021
14:59
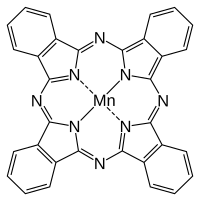
phtalocyanine de manganèse
Mode opératoire:
Manipulations à réaliser sous une hotte en fonction.
1/ dans un ballon monocol de 100 cm3, introduire 8.0 g d'éthanoate de manganèse tétrahydraté, 16.0 g de phtalonitrile et 40 cm3 de propan-1,2-diol. Ajouter quelques billes de verre pour l'agitation. Installer un réfrigérant à boules. Chauffer à reflux pendant 50 minutes.
éthanoate de manganèse trihydraté: 
phtalonitrile: 
2/ laisser refroidir lentement. Ajouter 100 cm3 d'eau. Filtrer sur fritté. Laver quatre fois avec à chaque fois 30 cm3 d'éthanol à 95° bouillant. Laisser sécher les cristaux, de couleur violette, en aspirant pendant 20 minutes puis à l'air (ne pas oublier d'enlever les billes de verre).
Published by jeanlouis.migot
-
dans
synthèse
20 mars 2021
6
20
/03
/mars
/2021
14:18
Published by jeanlouis.migot
-
dans
théorie
18 mars 2021
4
18
/03
/mars
/2021
15:17
réaction de Bouveault
Louis Bouveault
(1864 - 1909)

Mécanisme:
La première étape de cette synthèse est la formation d'un réactif de Grignard par réaction entre l'halogénure d'alkyle et du magnésium métallique. Cet organomagnésien subit ensuite l'addition d'un formamide N,N-disubstitutée (comme le DMF), formant un hémiaminal, ce dernier est ensuite facilement hydrolysé en l'aldéhyde désiré.
Published by jeanlouis.migot
-
dans
théorie
18 mars 2021
4
18
/03
/mars
/2021
08:37
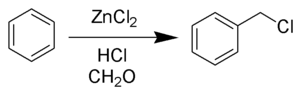
réaction de Blanc
Gustave - Louis Blanc
(1872 - 1927)
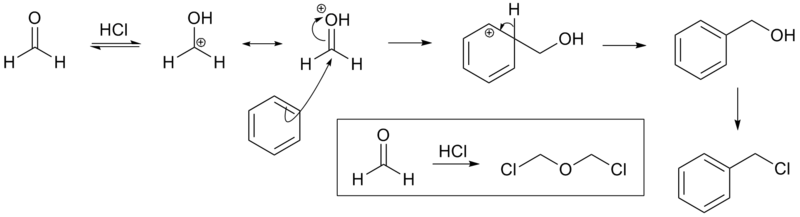
C'est la réaction chimique des cycles aromatiques avec le formaldéhyde et le chlorure d'hydrogène catalysée par le chlorure de zinc ou un autre acide de Lewis pour former des arènes chlorométhyliques:
Mécanisme:
Published by jeanlouis.migot
-
dans
théorie
17 mars 2021
3
17
/03
/mars
/2021
18:10
réaction de Blaise
Edmond Blaise
(1872 - 1939)
C'est une réaction organique de couplage qui permet de former un β-cétoester à partir de zinc métallique, d'un α-bromoester et d'un nitrile:
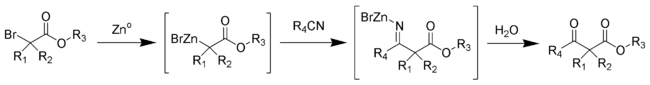
Mécanisme:
Il passe par la formation d'un organozincique complexe avec le brome en α du carbonyle de l'ester. Cela rend le carbone en α nucléophile, permettant une attaque électrophile du carbone du nitrile. L'azote alors chargé négativement du nitrile interagit avec le monobromure de zinc cationique. Le β-ènaminoester (tautomère de l'imine intermédiaire sur le schéma ci-dessus) est isolé lors d'un traitement du milieu réactionnel par une solution aqueuse à 50 % de K2CO3. Si le β-cétoester est le produit désiré, l'addition d'acide chlorhydrique molaire permet l'hydrolyse du β-ènaminoester en β-cétoester.
Published by jeanlouis.migot
-
dans
théorie
16 mars 2021
2
16
/03
/mars
/2021
18:23
le papier d'Arménie
À la fin du XIXème siècle, Auguste Ponsot, chimiste français, découvre lors d'un voyage que les Arméniens font brûler du benjoin, une résine qui vient de Malaisie, pour parfumer et désinfecter leurs maisons.
C'est un papier parfumé à la résine de benjoin du Laos (Styrax benzoin).
Le principal composant du benjoin est l'acide benzoïque pour le benjoin d'Indochine et l'acide cinnamique pour le benjoin de Sumatra. Ils contiennent également un petit pourcentage de vanilline. Le nom de benjoin est à l'origine de celui du benzène.
acide benzoïque: 
acide cinnamique: 
vanilline: 
D’abord le benjoin est macéré dans de l'éthanol, des feuilles de papier buvard passent dans les bacs d'eau salée (pour retarder la combustion) puis sont séchées avant d'être trempées dans le benjoin et placées en étuve. Le procédé permet au produit final de se consumer sans flamme.
Auguste Ponsot
(1846 - 1907)

Published by jeanlouis.migot
-
dans
origine
15 mars 2021
1
15
/03
/mars
/2021
20:10
réaction de Bamberger
ou
réarrangement de Bamberger
C'est une réaction chimique se produisant entre les N-phénylhydroxylamines et les acides forts dans l'eau. Elle a pour effet la formation de 4-aminophénols:
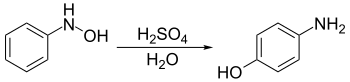
Mécanisme:
Le mécanisme du réarrangement de Bamberger consiste tout d'abord en la protonation de la N-phenylhydroxylamine 1. La N-protonation 2 est alors favorisée, mais inefficace. La O-protonation 3 peut former l'ion nitrénium 4, lequel peut réagir avec les nucléophiles (H2O) pour former le 4-aminophénol désiré 5:

Eugen Bamberger
(1857 - 1932)

Published by jeanlouis.migot
-
dans
théorie
15 mars 2021
1
15
/03
/mars
/2021
18:17
réaction de Zinine
ou
réduction de Zinine
Cette réaction implique la transformation d'un composé aromatique avec un groupement nitro comme le nitrobenzène en une amine aromatique par déduction avec le sulfure de sodium ou des sulfures métalliques comme l'aniline.
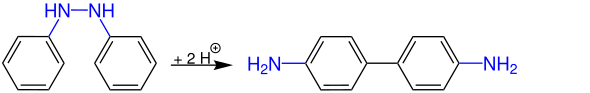
Mécanisme:

Nicolaï Zinine
(1812 - 1880)

Published by jeanlouis.migot
-
dans
théorie
13 mars 2021
6
13
/03
/mars
/2021
18:20
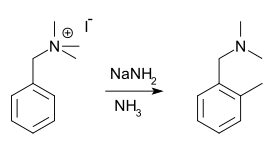
réaction de Ziegler
ou
alkylation de Ziegler
Karl Ziegler
(1898 - 1973)
Prix Nobel de Chimie 1963

Published by jeanlouis.migot
-
dans
théorie
13 mars 2021
6
13
/03
/mars
/2021
09:40
réaction de Wittig
1953
aldéhyde ou cétone ---vers---> alcène
C'est un cas particulier des additions nucléophiles. Il s'agit de l'addition d'un ylure de phosphore (phosphorane, souvent appelé réactif de Wittig) sur un composé carbonylé (aldéhydes et cétones) pour former des composés éthyléniques (éthylène substitué).
Cette réaction est ainsi très utilisée pour former des dérivés éthyléniques peu substitués, difficile à former par des réactions d'élimination, qui forment majoritairement les composés les plus substitués. Elle a de plus un très bon rendement, explicable thermodynamiquement par la formation de l'oxyde de triphénylphosphine qui possède une liaison P=O très forte (de l'ordre de 535 kJ·mol-1).
Georg Wittig
(1897 - 1987)
Prix Nobel de Chimie 1979

Published by jeanlouis.migot
-
dans
théorie




/image%2F0994837%2F20210323%2Fob_428264_img-3.gif)



/image%2F0994837%2F20210320%2Fob_ff32aa_img903.jpg)

/image%2F0994837%2F20210318%2Fob_acde88_img902.jpg)


/image%2F0994837%2F20210318%2Fob_f7aa2c_img900.jpg)


/image%2F0994837%2F20210317%2Fob_7bcd7a_img899.jpg)







/image%2F0994837%2F20210316%2Fob_9e7398_img898.jpg)



/image%2F0994837%2F20210315%2Fob_fb3dd4_img897.jpg)

/image%2F0994837%2F20210313%2Fob_6402a4_img896.jpg)

/image%2F0994837%2F20210313%2Fob_6d6679_img894.jpg)